ディープラーニングを活用した CT 撮影における放射線被ばくリスクの低減
著者 Dr. Ryohei Nakayama, Ritsumeikan University
コンピューター断層撮影 (CT または CAT スキャン) は臓器、骨、血管の 3D 画像を生成するため、単なるレントゲン写真よりもはるかに高い診断性能を有します。しかしそれと同時に、人体に有害である放射線の被ばく量が増えるという代償が伴います。CT スキャンでは、2D の X 線画像をコンピューター ソフトウェアで重ねて組み合わせることで 3D 画像を生成します。したがって、1 回の胸部 CT スキャンの平均実効線量は 7 ミリシーベルト (mSv) となり、胸部 X 線の場合の 0.02 mSv と比較すると 350 倍も高くなります。[1] 放射線被ばくは、がんのリスクにつながります。ガイドラインでは、小児への CT スキャンの線量は 1.5 mSv に制限されています。
医工学研究者は、医師に必要な画像の鮮明さを提供しながら、放射線被ばく量を抑えることを目指しています。有望視されている 1 つのアプローチは、超低線量 CT を使用する方法です。この方法では 1 回の胸部画像の平均実効線量が約 0.13 mSv となります。[1] 超低線量 CT スキャンの主なデメリットは、解像度が比較的低く、ノイズが多くなるため、臓器、脂肪、間質組織が見えにくくなることです (図1)。
筆者は、超低線量 CT スキャンを入力として使用しながら通常線量の CT スキャンと同程度の画質の画像を生成する、畳み込みニューラル ネットワーク (CNN) 回帰をベースとした MATLAB® ソフトウェア システムを開発しました。このシステムでは同程度の診断情報を提供しながら、患者の放射線被ばく量を最大 95% 低減します。
超解像処理と CNN の比較
低線量 CT の画質を向上させる方法として、初めに超解像技術を適用しました。このアプローチでは MATLAB を使用し、CT 画像を小さな局所領域の画像に分割して、低線量の領域と通常線量の領域をペアにすることで画像ディクショナリを作成しました。このシステムで新しい低線量画像を分析する際は、このディクショナリの中から類似した低線量領域を検索し、それに対応する通常線量の画像をユーザーに表示します。
この方法の有効性は、比較対象を取得するための大きなディクショナリがあるかどうかに左右されます。しかし、ディクショナリのサイズが大きくなると、システムリソースへの要求が増え、さらに重要なことには、類似した低線量領域を見つけるための検索時間が長くなります。CNN は学習に時間がかかりますが、新しい画像を提示されたときに結果を生成するスピードが、筆者の開発した超解像処理アプローチよりもはるかに速くなります。一例として、学習済み CNN では 1 人の患者の結果を約 20 分で得られるのに対し、超解像処理を使用した場合は同等の結果を得るために約 2 時間かかりました。
超解像処理の欠点に対処するために CNN 回帰の検討を始めたところ、超解像処理の方が非常に優れているケースもありました。たとえば、診断する画像のパターンがディクショナリ内のある画像に非常に似ている場合、超解像処理によるアプローチは非常に正確な結果を生成します。そのため、CNN 回帰と超解像処理を組み合わせたハイブリッド システムの構築を計画しました。
画像の入手と CNN の構築
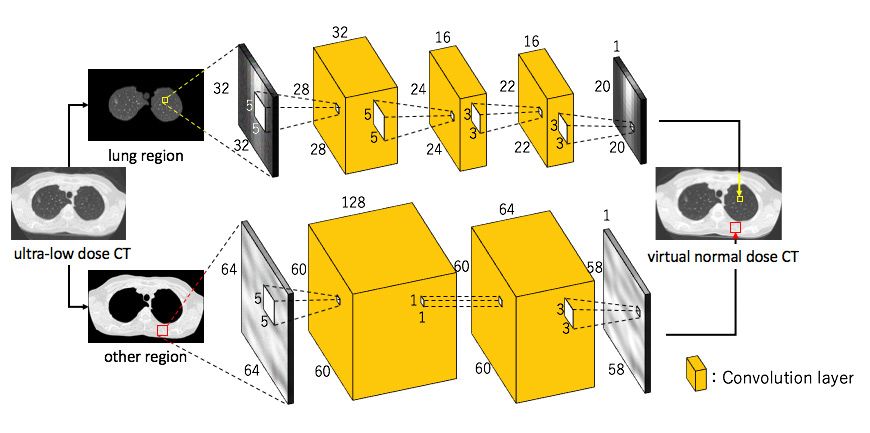
超低線量胸部 CT スキャンの鮮明度を向上させるため、2 つの CNN を使用するアプローチを採用しました。1 つは CT 画像の肺の領域を対象としたもので、もう 1 つは肺以外の領域を対象としたものです (図 2)。CNN の学習に使用した画像データセットは、三重大学の研究チームから提供を受けました。このデータセットは 12の画像ペアで構成されており、各画像ペアには同じ患者の通常線量のスキャンと超低線量のスキャンが含まれています (追加で超低線量の画像を撮影することで患者の被ばく量が増えるため、今回の研究では被験者を比較的少なく制限しました)。各画像は 512 x 512 ピクセルで、各スキャンには 250 枚の画像 (断層) が含まれています。
CNN の初期構造は、超解像処理での結果を踏まえたものとしました。筆者が行った超解像処理の研究では、7 x 7 サイズの局所領域で最適な結果が得られることがわかっています。そこで、ディープラーニング モデルではそのサイズの局所領域を使用することから始めました。その後、局所領域を 5 x 5 と 128 x 128 の間で変えながら実験し、それぞれが生成する結果の鮮明度を確認したうえで、肺の領域では 32 x 32、肺以外の領域では 64 x 64 を設定しました。また、MATLAB で入力サイズとフィルター、畳み込み層の数を変えた128 種類の異なるCNNを評価しました。
CNN の学習と検証
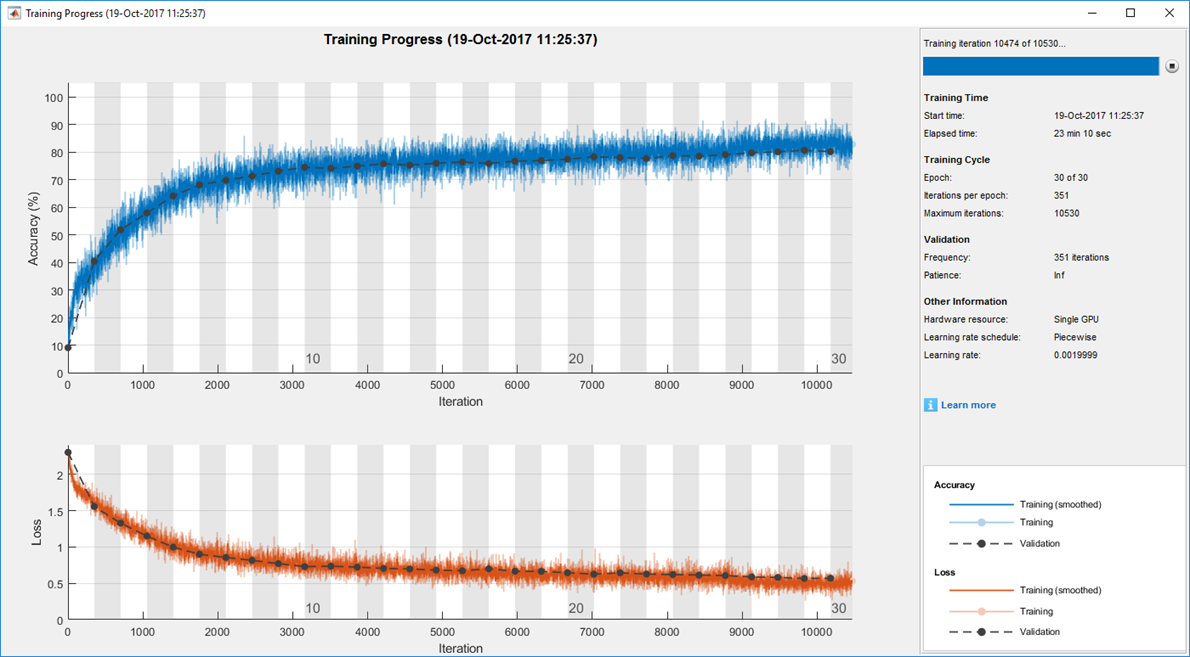
交差検証を用いて、11 人の患者の画像を使用してモデルの学習を行い、残った 1 人の患者の画像を使用して評価しました。学習セットと評価画像を入れ替え,この手順を 12 回繰り返しました。過程を迅速に進めるため、Parallel Computing Toolbox™ を使用して複数の NVIDIA® GeForce シリーズの GPU で並列に学習を行いました。学習の進行状況をモニタリングするため、Deep Learning Toolbox™ のモニタリング可視化機能で精度と損失をプロットしました (図 3)。
それぞれの超低線量テスト画像の結果は、対応する通常線量画像に照らして、二乗平均平方根(RMS) レベルと画質のメトリクスを測定するための構造類似性指数 (SSIM) を用いて評価しました。
次のステップ
今回の CNN ベースのシステムを実際の臨床環境で使用する計画を立てています。また、医療用画像管理システム (Picture Achieving and Communication; PACS) サーバーにこのシステムを導入して、医療画像を簡単に保存したりアクセスしたりできる方法も模索しています。MATLAB で医療画像処理ソフトウェアを開発するメリットは数多くあります。たとえば、以前に開発した他の MATLAB ベースのシステムでも行ったように、基礎となるアルゴリズムへのインターフェイスを作成して全体のパッケージを医師に配布するというプロセスが簡単になる環境です。
立命館大学は全校規模で MATLAB と Simulink を利用している世界中で 1,000 校を超える大学の 1 つです。Total Academic Headcount (TAH) ライセンスを導入しており、研究者、教職員、学生が最新リリースレベルの製品の共通のコンフィギュレーションを、講義室や自宅、研究室、現場などあらゆるところで使用しています。
公開年 2018
参照文献
-
"What are the Radiation Risks from CT?" U.S. Food and Drug Administration. https://www.fda.gov/radiation-emitting-products/medical-x-ray-imaging/what-are-radiation-risks-ct
-
Wang R, et al. "Ultralow-radiation-dose chest CT: accuracy for lung densitometry and emphysema detection." American Journal of Roentgenology (2015). 204: 743-749. 10.2214/AJR.14.13101. https://pubmed.ncbi.nlm.nih.gov/25794063/